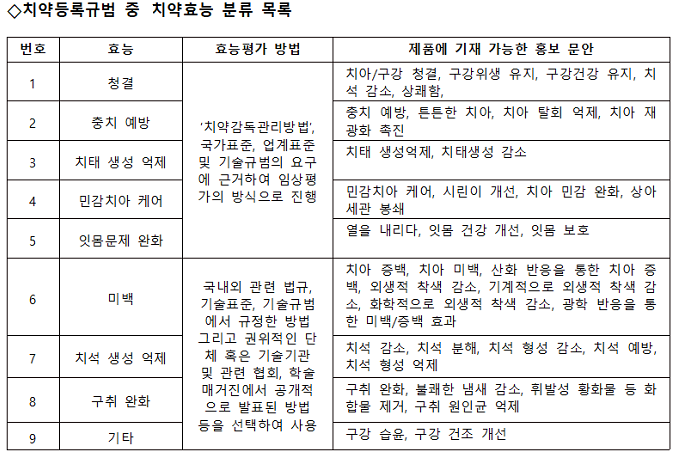
중국 NMPA(국가약품감독관리국)에서는 13일 ‘치약등록규범’을 발표하고 의견조회를 요청했다고 대한화장품협회가 밝혔다.
’21년 1월 1일부터 시행 중인 ‘화장품감독관리조례’에서는 치약이 화장품 정의에 포함되지 않지만 화장품에 준해 관리하기 위해 ‘치약감독관리조례’를 발표한 바 있다. 이 조례는 전 23조이며 시행일은 의견 수렴 후 발표될 예정이다.
치약 관련해서 지난해 8월 25일 중국구강청결케어용품협회가 “치약 중 기사용한 원료 현황 수집 통지를 발표하고 각 기업에서 회신한 내용에 근거해 ‘치약 기사용원료목록’을 제정한다”고 발표한 바 있다.
지난해 11월 13일 NMPA에서는 ‘치약감독관리방법’(의견수렴안)을 발표하고 ▲치약의 신원료 판단 여부에 대한 기준(치약 기사용원료목록)을 제시했으며, 제품 등록 시 필요한 서류, 치약의 효능 분류 및 제품명 명명 기준, 효능평가 및 관련 시험 기관에 대한 요구 등을 제시했다.
이번에 공개된 ‘치약등록자료규범’(의견조회안)은 △1장 총칙 △2장사용자 정보 관련 자료 요구 사항 △3장 등록자료에 대한 요구 △4장 변경사항에 대한 요구 △5장 말소 등 사항에 대한 요구 △6장 부칙 등 전 53조로 구성돼 있다. 별첨으로 △치아 효능 분류 목록 △치약 등록 검사 요구 △치약 등록 검사보고서 요구 △등록인 정보표 △품질관리체계 개요 △부작용 모니터링 및 평가시스템 개요표 △경내책임자 정보표 △치약 등록 경내책임자 수권 및 승낙서 등 각종 서류 양식이 첨부됐다.
이에 대해 중국 정부의 공식 시험·검역·등록·교육서비스 기관인 씨에이아이큐테스트(CAIQTEST Korea, 检科测试) 김주연 본부장은 “중국의 대표적인 치약 관련 표준은 〈GB 8372 치약〉 〈GB 22115 치약원료규범〉이며, 이 표준을 참고하여 기사용원료목록과 관련 규정들이 발표 및 시행될 것”이라고 전망했다.
이어서 김 본부장은 “‘치약등록관리규범’ 중 주요 내용은 ▲치약제품 등록 서류는 화장품과 동일하나 제품 효능 관련해서는 제품 특성에 맞게 구분 ▲사용군에 따라 성인 및 아동(6개월~12세)으로 나뉘며 ▲아동용 제품은 ①청결 ②충치 예방의 효능만 홍보가 가능하다”고 설명했다.
중국 수출을 준비하는 국내기업이라면 기존 화장품 등록 절차와 구비서류를 참고하되 새롭게 발표될 규정을 전문기관과 함께 대응해야 한다고 업계 전문가는 조언했다.